近年来,癌症相关成纤维细胞(Cancer-associated fibroblasts,CAFs)在肿瘤微环境(Tumor microenvironment,TME)中的作用日益受到关注。CAFs不仅影响肿瘤进展,还显著影响其治疗效果。成纤维细胞曾被视为简单的结构细胞,主要参与细胞外基质沉积和组织修复。然而,近年来的研究表明,成纤维细胞在病理条件下表现出前所未有的可塑性和功能异质性,能够显著影响周围细胞及其微环境中的不同过程。在癌症中,成纤维细胞已成为肿瘤微环境的关键组成部分,对癌症进展和治疗反应产生重要影响。CAFs的异质性已被证实在肿瘤中发挥双重作用,既有肿瘤抑制作用,也有肿瘤支持作用。最新的研究甚至表明,成纤维细胞中的突变也可能导致癌症的发生,进一步强调了其在肿瘤发生中的重要作用。此外,单个肿瘤中存在多种具有不同功能的成纤维细胞亚型。因此,对CAFs的深入研究对于理解肿瘤的发生和发展具有重要意义。
2024年,国外Maria Kasper 和 Beate M. Lichtenberger团队在Nature Communications上发表了一篇题为Cancer-associated fibroblast subtypes modulate the tumor-immune microenvironment and are associated with skin cancer malignancy的研究论文。本研究使用敏感的 Smart-seq2 scRNA-seq 技术(n= 10个肿瘤样本)和 mRNA 原位染色(n= 68个肿瘤样本)研究了基底细胞癌(BCC)、鳞状细胞癌(SCC) 以及黑色素瘤三种癌症的细胞生态系统——重点关注并展示了成纤维细胞的异质性,同时发现mCAF亚型在肿瘤-基质边界形成致密的细胞外基质网络,可能在T细胞边缘化中发挥作用,并提出iCAF亚型是免疫细胞募集和免疫监视的重要调节因子。
文章主要结果和发现
一:原发BCC,SCC以及黑色素瘤的单细胞图谱
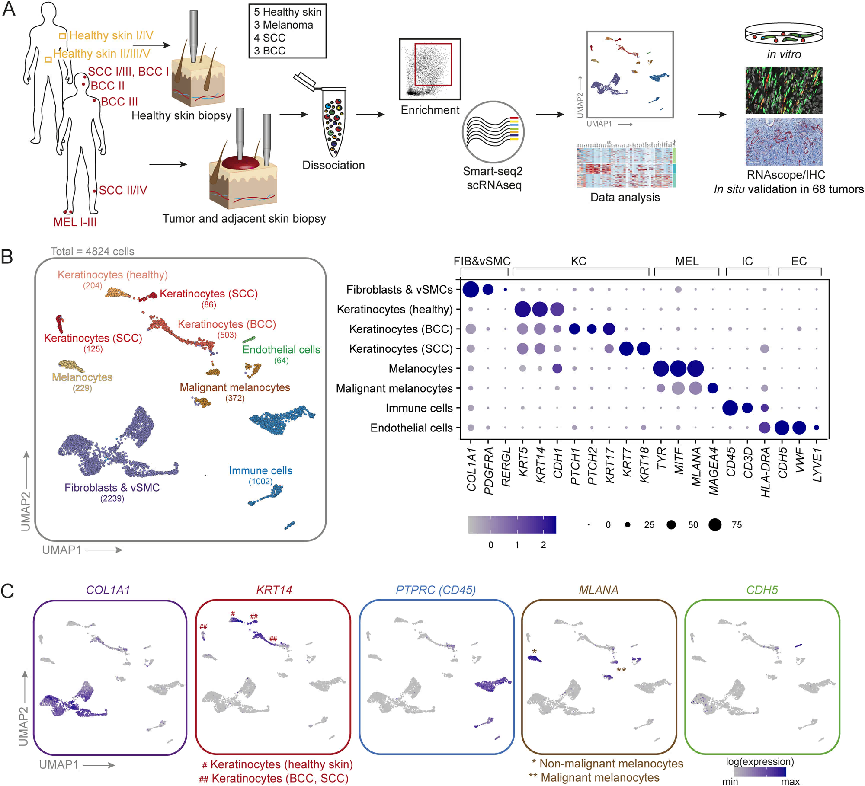
为探讨成纤维细胞的异质性及其与肿瘤细胞和免疫细胞的相互作用,研究收集了4例鳞状细胞癌、3例基底细胞癌、3例黑色素瘤以及5例健康供者皮肤样本。使用流式分选方法来富集角质形成细胞、成纤维细胞和免疫细胞并利用Smart-seq2 技术进行测序(Fig1A)。无监督聚类将细胞分离成纤维细胞、健康和恶性角质形成细胞以及黑色素细胞、免疫细胞和内皮细胞。细胞类型定义基于普遍接受的特征基因表达:成纤维细的COL1A1和PDGFRA,血管平滑肌细胞(vSMC)的RERGL,角质形成细胞的KRT5、KRT14和CDH1 (E-cadherin),免疫细胞的PTPRC(CD45),黑色素细胞TYR、MITF和MLANA以及内皮细胞的CDH5(Fig1B、C)
二:非间充质细胞二级聚类及CNV分析
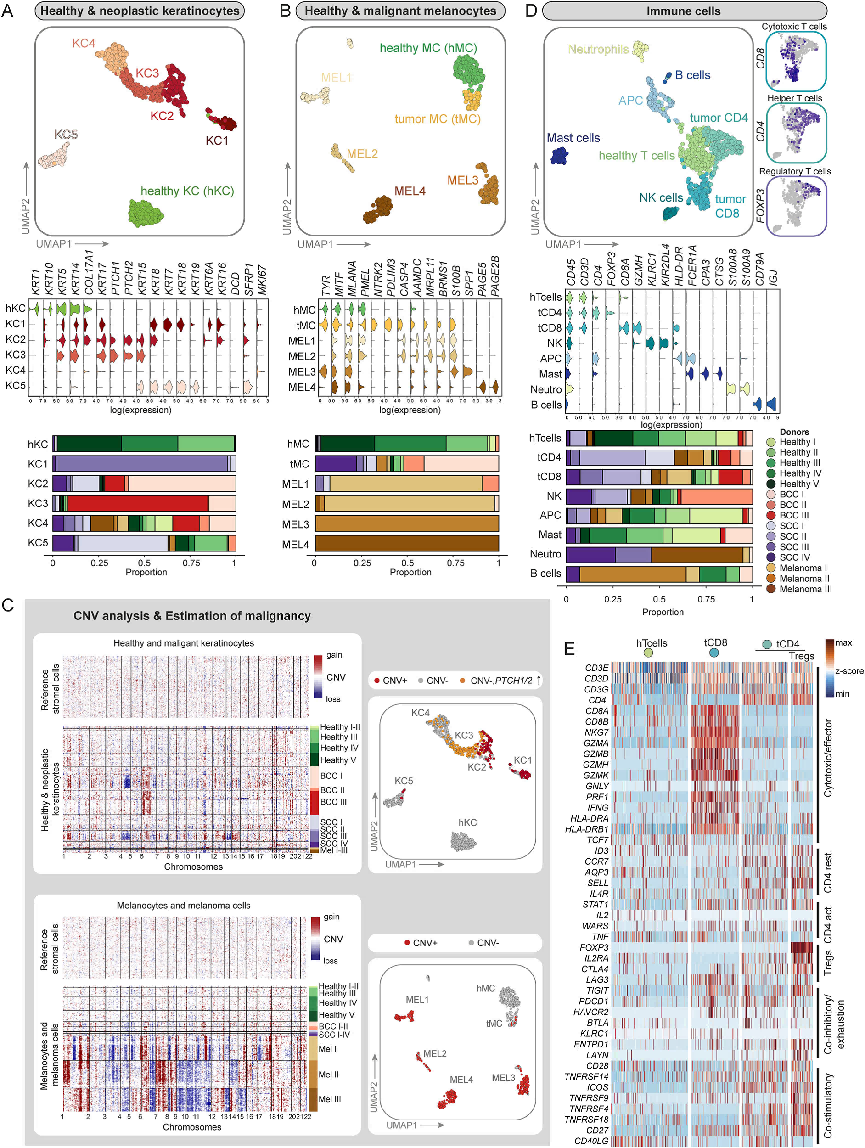
鳞状细胞癌与基底细胞癌均来自于角质形成细胞的癌变,黑色素瘤来源于黑色素细胞癌变,因此在第一部分内容分析BCC,SCC,黑色素瘤细胞生态图谱后,研究团队将目光聚焦于角质形成细胞以及黑色素细胞。健康角质形成细胞和肿瘤角质形成细胞的二级聚类导致明显分离的健康角质形成细胞簇(hKC)具有基础(KRT5、KRT14、COL17A1)以及分化(KRT1、KRT10)标记基因表达。
肿瘤细胞表达一系列健康皮肤角质形成细胞不表达的额外角蛋白(Fig2A)。通过对健康黑色素细胞以及黑色素瘤细胞的二级聚类分析,黑色素瘤样本被分成四个不同的供体特异性簇:MEL1和MEL2来自黑色素瘤I,MEL3来自黑色素瘤II,MEL4来自黑色素瘤III(Fig2B)。为了解释黑色素瘤细胞所出现的供体特异性聚类,本研究对黑色素细胞和黑色素瘤细胞进行了拷贝数变异(CNV)分析,并对健康和恶性角质形成细胞进行了单独的CNV分析,使用健康的基质细胞(成纤维细胞、血管平滑肌细胞和周细胞)作为参考。由于非恶性细胞在几乎所有供体样本中混合,如tMC或免疫细胞(图2B-D),因此,供体特异性肿瘤细胞在KC1和MEL1-MEL4中的聚集可能是基因组畸变的结果,而不是批次变异的影响。通过对免疫细胞的二级聚类分析,其结果包括T细胞和B细胞、粒细胞和抗原呈递细胞的等8个免疫细胞簇(Fig2D),有趣的是来自健康样本的CD4和CD8T细胞(hTcells)形成了一个与CD4相邻的独特的簇,这可以通过健康或肿瘤样本中T细胞的不同激活状态来解释:颗粒酶、穿孔素和IFNγ的表达增加表明肿瘤样本中的CD8T细胞与健康组织中的CD8T细胞活化(Fig2E)。
三:成纤维细胞和血管平滑肌细胞(vSMCs)的二级聚类导致两个健康的成纤维细胞群体、四个CAF亚群和一个vSMC聚类
成纤维细胞的亚聚集分析将健康皮肤的成纤维细胞与CAF分开聚集,二级聚集包括7个子聚集。本研究从健康皮肤样本中分类了两个主要簇,称为乳头状成纤维细胞(pFIB)和网状成纤维细胞(rFIB),四个CAF子簇称为基质CAF (mCAF)、免疫调节CAF(iCAF)、RGS5+CAF和RGS5+周细胞、以及不可分类的CAF(ucCAF)和一个vSMC簇,每一簇使用差异表达基因以及普遍接受的标记来定义这些亚簇(Fig3A)。与所有其他成纤维细胞簇相比,基质CAF(mCAF)表现出细胞外基质成分的表达增加,例如胶原蛋白(COL1A1、COL1A2、COL3A1)、Lumican(LUM)、Periostin (POSTN)或 Tenascin-C(TNC),免疫调节CAFs(iCAFs)在其前十大差异表达基因中表现出基质重塑因子MMP1和MMP3、促炎细胞因子IL6和CXCL8以及免疫抑制分子IDO1的表达增强,因此表明iCAF可能与免疫调节和癌症侵袭有关(Fig3B、C)。由拟时序分析的结果可以看出健康的成纤维细胞遵循两条分化途径:走向mCAF/iCAF或走向RGS5+细胞。轨迹分析还表明,iCAFs是一个差异化终点,mCAFs是中间状态,因此 iCAFs有可能从mCAF发展而来(Fig3D、E)
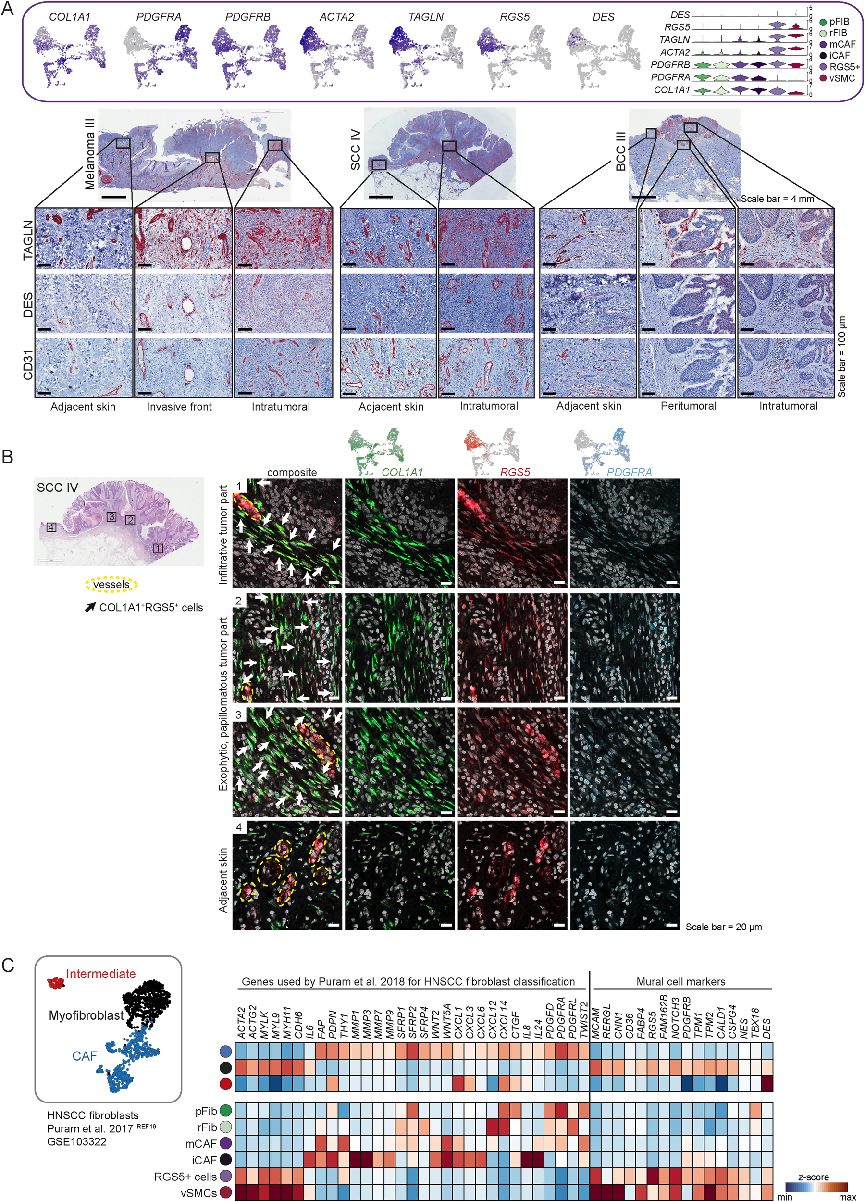
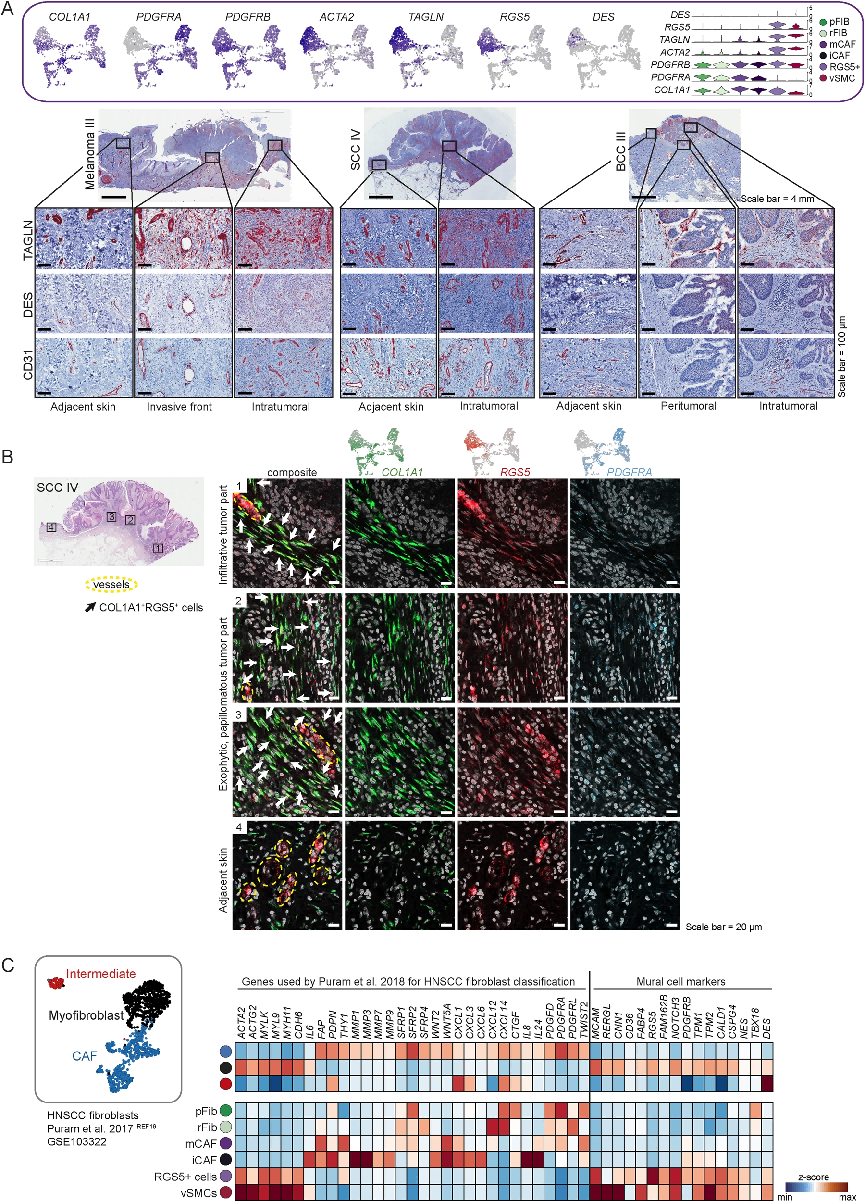
四:RGS5+细胞是CAF和周细胞的不均匀群体
当研究不同CAF亚型的详细基因表达谱时,研究者们怀疑RGS5+簇可能同时包含myCAFs和周细胞,因为RGS5+细胞表达ACTA2(Fig4A),该研究为了进一步表征RGS5+簇的性质,对肿瘤切片进行TAGLN染色,TAGLN是该簇中显著表达的基因。组织染色显示TAGLN蛋白如预期的那样沿着血管,但也在肿瘤基质内,没有直接接触血管样结构(Fig4A),接下来该研究又对RGS5、COL1A1和PDGFRA mRNA进行了共染色,验证RGS5+细胞在基质和血管周围的存在。在肿瘤区域,血管结构和间质内均检测到RGS5阳性染色,而在肿瘤周围区域,RGS5仅在血管样结构周围检测到(Fig4B)。为了阐明肿瘤样本中细胞myCAFs 或周细胞的差异分类,本研究重新分析了公开可用的头颈部鳞状细胞癌(HNSCC)数据集,并将其与该研究的数据集进行比较,通过普遍接受的周细胞标记物扩展了他们已发表的标记基因集,发现仅在肌成纤维细胞簇中富集的标记基因,揭示了与RGS5+细胞簇非常相似的表达谱(Fig4C)。
五:mCAFs和iCAFs分别以表达ECM和免疫调节基因为特征
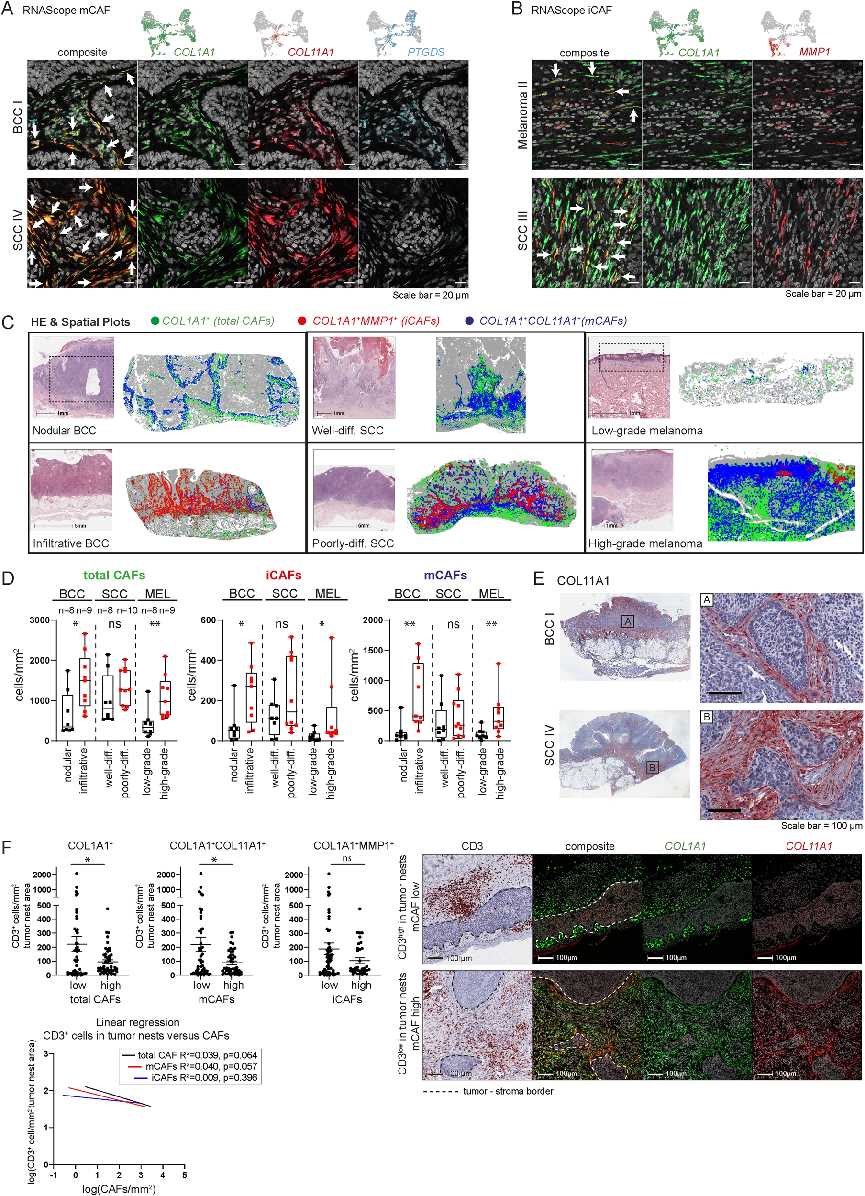
接下来,该研究通过mRNA原位染色对mCAF和 iCAF亚群的存在和空间定位进行验证。使用COL11A1和PTGDS作为mCAF的标志物,使用MMP1作为iCAF的标志物,mCAFs 大量存在于包裹肿瘤巢的大块中,但也以股状形式分布于肿瘤中(Fig5A)。相反,在MMP1COL1A1+细胞之间的瘤内基质巢和弥漫肿瘤的细胞链或侵袭前的斑块中发现了较少数量的iCAF(Fig5B)。为了验证 scRNA-seq数据表明iCAFs在侵袭性肿瘤中占主导地位,将肿瘤样本分为不同的类别:结节性和浸润性BCC、高分化和低分化SCC,以及低级别和高级别黑色素瘤,肿瘤组织样本中CAF亚群的空间可视化显示,CAF模式从低恶性到高恶性明显变化,同时在各自皮肤癌亚型的侵袭性变异中,CAF总密度更高(Fig5C)。为了量化CAF亚群的差异,在肿瘤内以及侵袭前设置了感兴趣区域。浸润性黑素瘤的总CAF密度显著高于结节性黑素瘤,高级别黑素瘤的总CAF密度显著高于低级别黑素瘤。此外,iCAFs在结节性BCC和浸润性BCC之间,以及低级别(≤T1)和高级别(≥T3)黑色素瘤之间的数量也分别增加,有趣的是,与结节性黑素瘤相比,浸润性黑素瘤中mCAFs的丰度增加,高级别黑素瘤(≥T3)与低级别黑素瘤(≤T1)的mCAFs丰度增加(Fig5D)。COL11A1蛋白染色显示在肿瘤巢的基底膜上排列着密集的胶原纤维网络(图5E),表明mCAFs可能控制T细胞边缘化。同时研究量化了总癌组织(包括肿瘤间质)中mCAFs和CD3+细胞的数量,以及每个结节性和浸润性BCC样本中几个肿瘤巢内CD3+细胞的数量。mCAFs/ mm²组织数量与肿瘤巢内CD3+细胞/mm²呈负相关(图5F),提示mCAFs可能形成物理屏障,抑制T细胞浸润肿瘤巢。
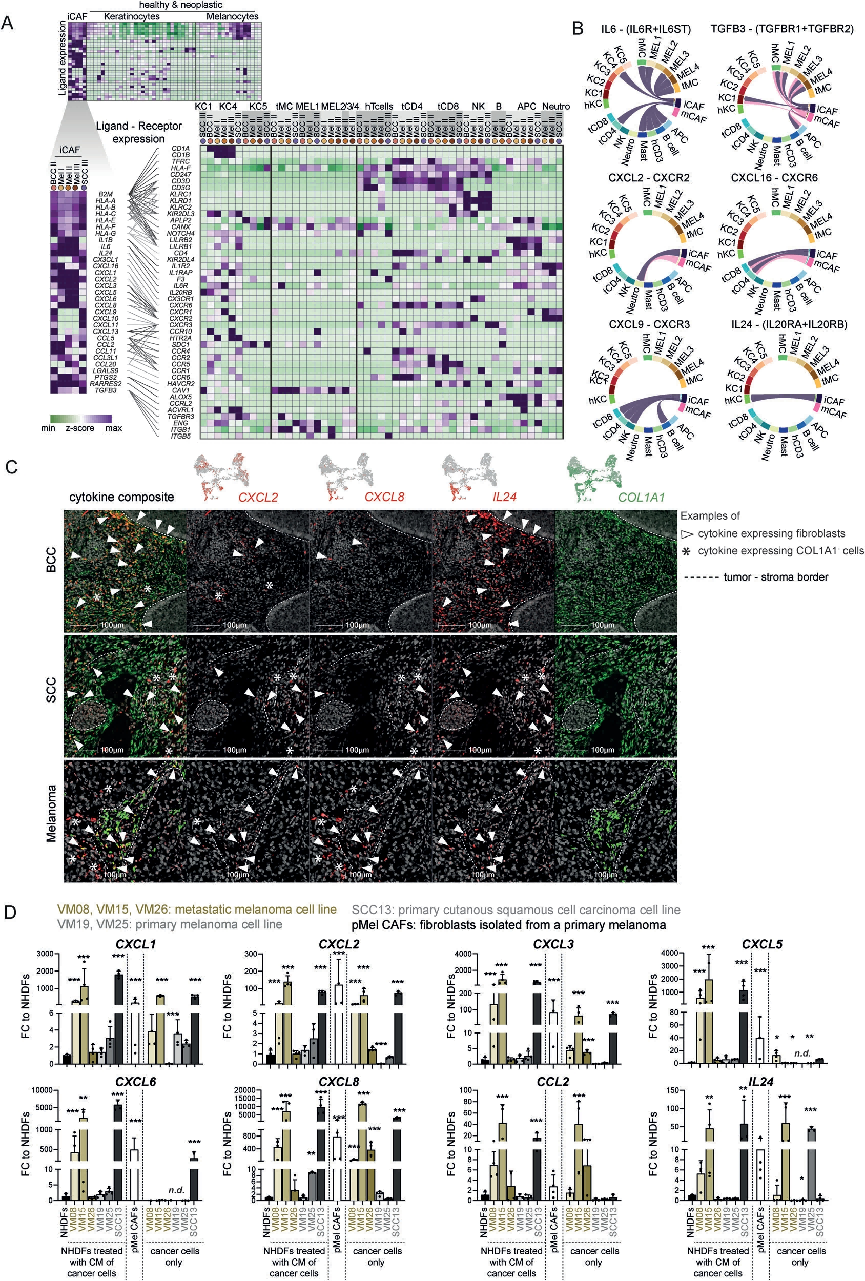
六:成纤维细胞是肿瘤中趋化因子的重要来源
iCAFs强烈表达的免疫调节基因包括TGFB3和LGALS9,促炎细胞因子如IL1B和IL6。此外,与健康或肿瘤角质形成细胞和黑色素细胞相比,iCAFs表达了大量的趋化因子,因此可能调节免疫细胞组成并影响肿瘤中的免疫监视,因为它们的受体存在于许多不同的免疫细胞上。值得注意的是,来自黑色素瘤样本的iCAFs表达了高水平的CXCL1-8,但不表达CXCL9-13。而CXCL9-13在SCC III和BCC II样本的iCAFs中表达较高。只有CXCL2在所有肿瘤样本的iCAF中同样高表达。同样,IL1B在黑色素瘤的iCAFs中表达水平更高,而TGFB3和LGALS9在BCC和SCC的iCAFs中强烈表达,但在黑色素瘤中不表达,通过mRNA原位染色进一步证实了CAF衍生的细胞因子表达(Fig6A,B)。虽然大多数结节性BCC和低级别黑色素瘤中没有或没有单个分散的表达细胞因子的CAFs,但一些浸润性BCC和高级别黑色素瘤中存在多簇表达细胞因子的CAFs,这与原位定量的iCAFs相一致(Fig6C)。有趣的是,来自黑色素瘤转移瘤或高度侵袭性SCC的培养细胞系的条件培养基强烈诱导NHDFs中不同细胞因子和趋化因子的表达。同样,这些细胞因子和趋化因子在未进一步治疗的原发性黑色素瘤中分离的成纤维细胞中也有高水平表达(Fig6D)。
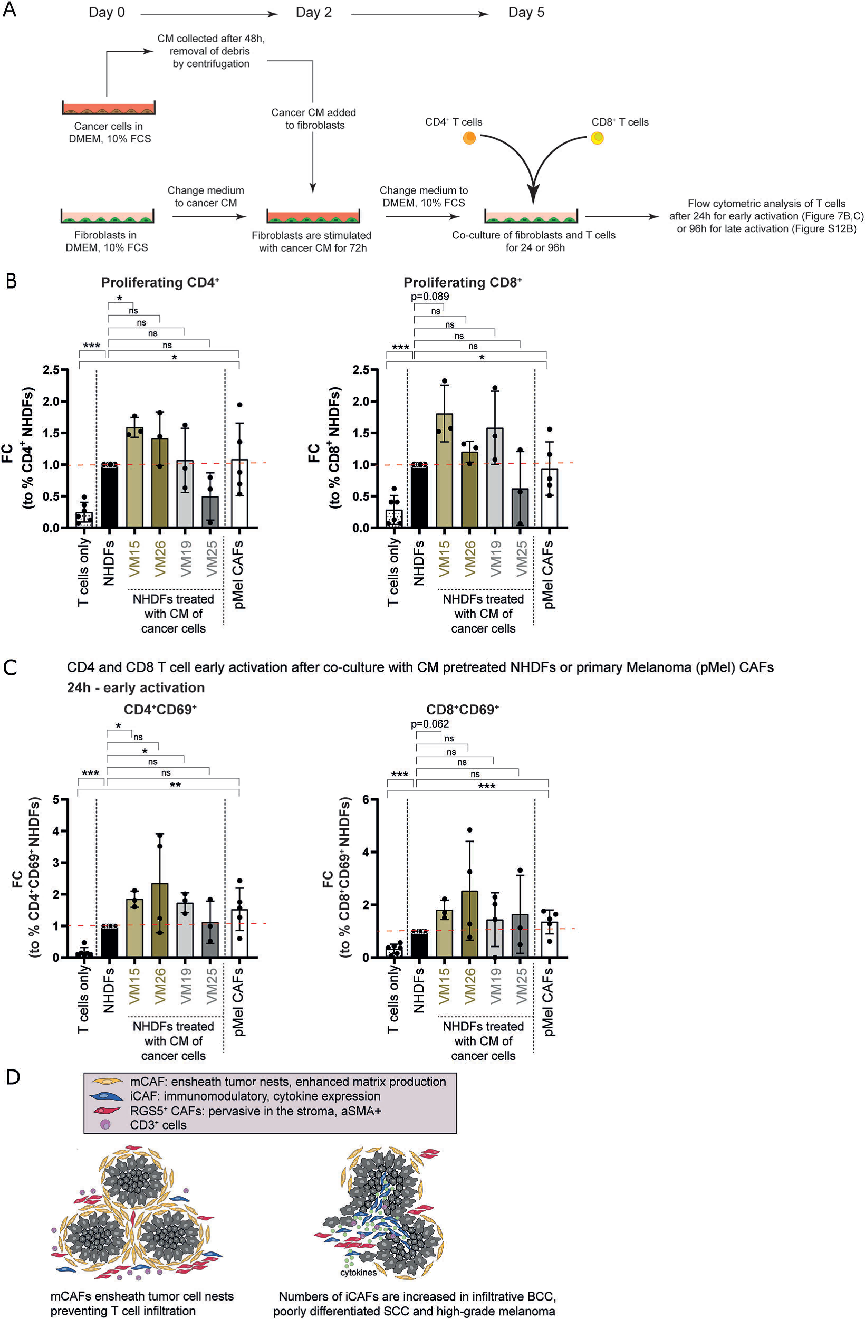
七:成纤维细胞激活CD4+和CD8+T细胞
将naïve CD4和CD8T细胞与用VM15、VM26、VM19、VM25或对照培养基预处理的pMEL CAFs共培养,同时,将naïveCD4和CD8T细胞与癌细胞直接共培养。研究发现,从健康皮肤中分离的原代成纤维细胞能够激活T细胞(Fig7A-C),正如增殖的CD4和CD8T细胞的百分比增加(Fig7B)和活化的CD69+CD4和CD8T细胞的百分比所示。CD4 T细胞的VM15和VM19来源的CM促进了早期T细胞的激活,CD8 T细胞的VM15来源的CM促进了早期T细胞的激活(Fig7B)。综上所述,在我scRNA-seq筛选中鉴定的标记基因的原位染色显示,mCAFs和iCAFs是不同的CAF群体,遵循不同的原位分布模式(Fig 7D)。
总结:
此项研究提供了三种最常见的皮肤癌类型的细胞和分子图谱,包括肿瘤上皮细胞、间充质细胞和免疫细胞。并进一步揭示和表征了三个不同的CAF亚群,并表明它们的丰度和相关的信号分子和结构蛋白对TME有重要影响。
因此,确定肿瘤样本中的主要CAF亚群可能会改善未来的诊断策略,从而为更好的个性化治疗开辟新的途径。此外,药理学上靶向CAF以降低ECM密度可以增强T细胞向肿瘤巢的运输,从而提高检查点抑制治疗的效果以及直接靶向癌细胞的药物的渗透。
供稿:周丹娅、陈昭宇
参考文献:Forsthuber A, Aschenbrenner B, Korosec A, Jacob T, Annusver K, Krajic N, Kholodniuk D, Frech S, Zhu S, Purkhauser K, Lipp K, Werner F, Nguyen V, Griss J, Bauer W, Soler Cardona A, Weber B, Weninger W, Gesslbauer B, Staud C, Nedomansky J, Radtke C, Wagner SN, Petzelbauer P, Kasper M, Lichtenberger BM. Cancer-associated fibroblast subtypes modulate the tumor-immune microenvironment and are associated with skin cancer malignancy. Nat Commun. 2024 Nov 8;15(1):9678. doi: 10.1038/s41467-024-53908-9.