
由皮肤病学教育部重点实验室四个分中心暨北京分中心(中日友好医院),上海分中心(复旦大学附属华山医院),苏州分中心(苏州大学附属第四医院)和海南分中心(博鳌超级医院)合作完成的芦可替尼乳膏治疗中国非阶段型白癜风疗效和安全性的真实世界研究”论文日前在线发表在皮肤科SCI排名第一杂志《Journal of the American Academy of Dermatology》(影响因子12.8)。论文报告了国际上首个外用Janus激酶(JAK)抑制剂芦可替尼乳膏在治疗中国非节段型白癜风患者中的真实世界疗效与安全性数据。研究结果显示,芦可替尼乳膏有望成为中国非节段型白癜风患者的治疗选择之一。
白癜风是一种常见的色素脱失性疾病,我国近2000万患者,严重影响人类“颜值”和身心健康,现有治疗方法疗效有限。2022年美国FDA和2023年欧盟EMA批准外用JAK1/2抑制剂—1.5%磷酸芦可替尼乳膏治疗面部非节段型白癜风,这是国际上第一个有治疗白癜风适应症的外用药,其有效性和安全性已经在多个临床试验中得到了评估,但在中国人群中尚未有数据报道。
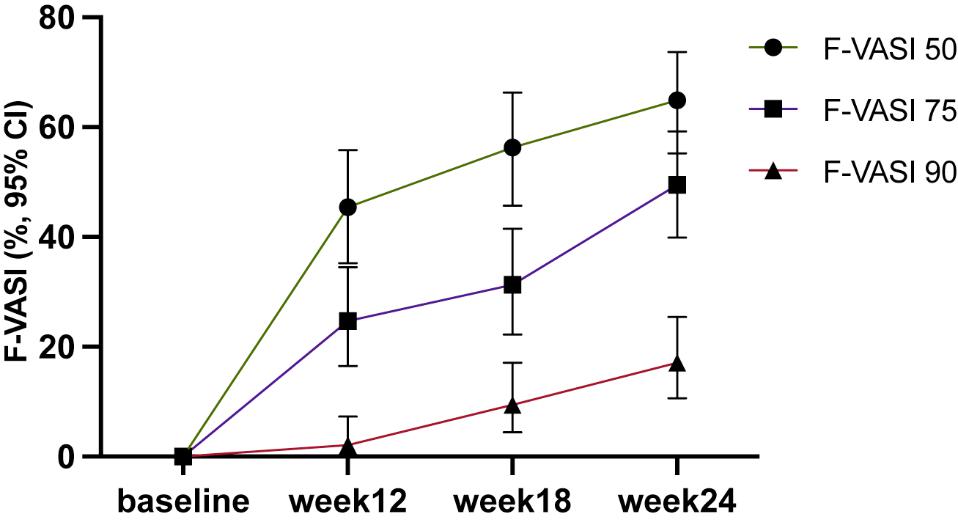
为评价其治疗中国非节段性白癜风患者的有效性和安全性,2023年8月国家药监局批准在海南博鳌乐城医疗先行区博鳌超级医院先行先试,开展了一项回顾性单臂,单中心的真实世界研究。研究共纳入111例非节段性白癜风且年龄≥12岁的患者,受试者白癜风受累面积(BSA)≤10%且面部白癜风面积评分指数(F-VASI)评分≥0.5。在24周时,49.5%的患者达到F-VASI 75,达到F-VASI50,和F-VASI90分别为64.9%和17.1 %。此外,还有13.6%的患者达到T-VASI 50。其中最常见的不良事件是用药部位轻度瘙痒、痤疮及脱皮。论文第一作者为黄贺(安徽医科大学),盛宇俊(中日友好医院)和李敏(苏州大学),通讯作者为张博(苏州大学),周幼文(UBC)和崔勇(中日友好医院)。
这是海外进口外用药第一个在我国开展的真实世界研究案例,国家药监局2024年6月批准依据芦可替尼乳膏疗效和安全性的真实世界研究数据作为在中国上市证据。
供稿:黄贺 皮肤病学教育部重点实验室
